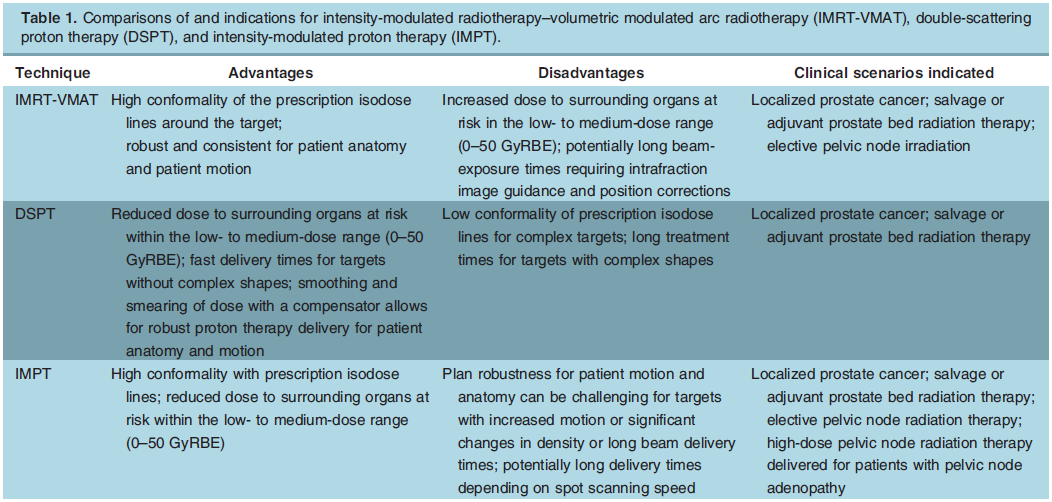
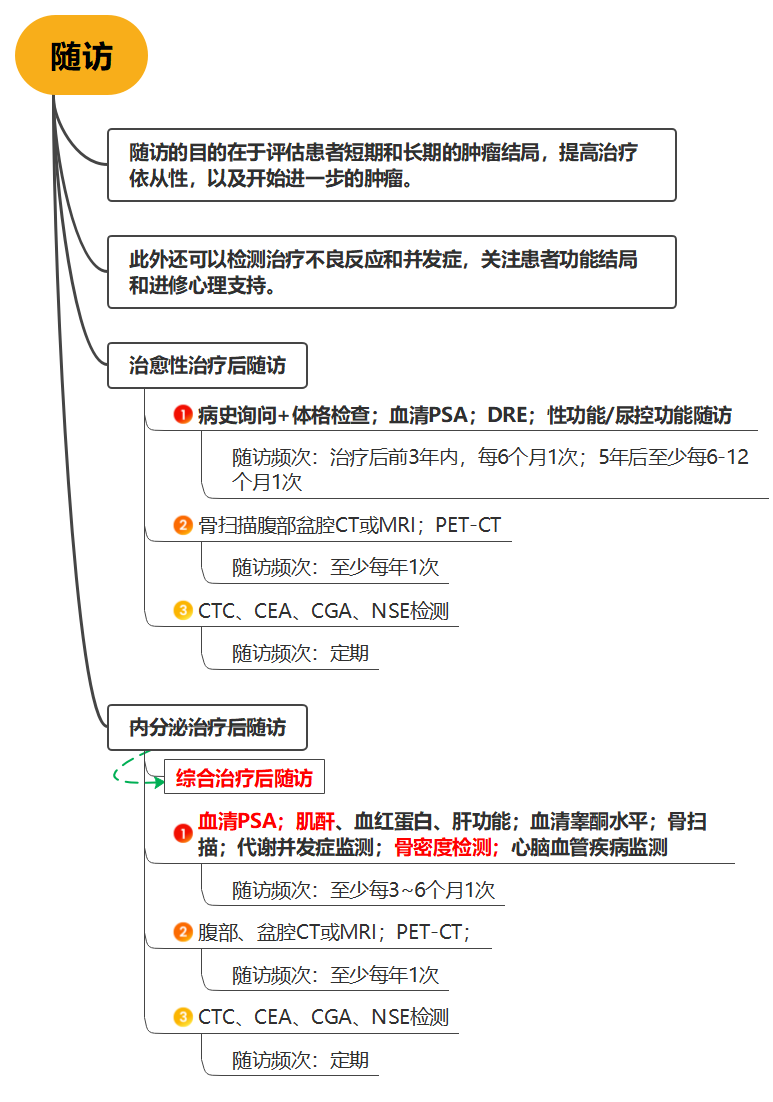
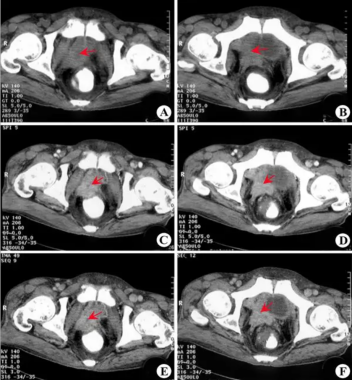
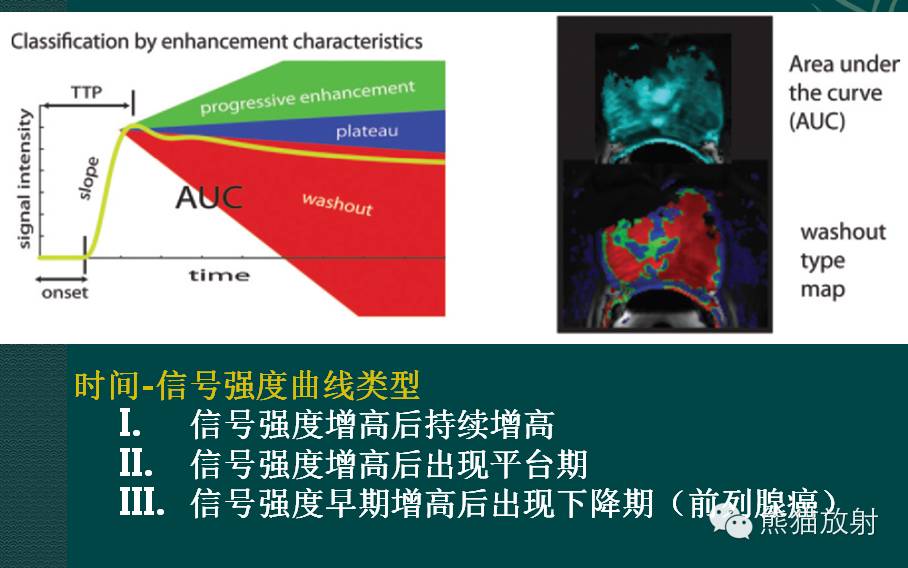
放射治疗是前列腺癌的主要治疗手段之一,前列腺癌的放疗方式有多种,立体定向放疗(SBRT)是近几年临床研究的热门。
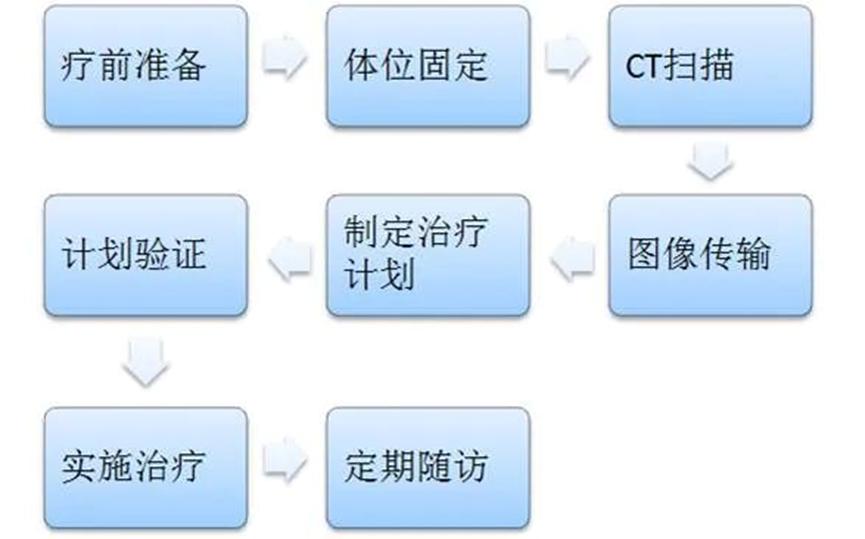
相比于传统的常规放疗,SBRT的特点是对定位要求更高,单次放疗剂量更大,但放疗次数较少。研究表明,前列腺癌对SBRT具有高度敏感性,改变肿瘤放疗的分割模式使得前列腺癌放疗的疗效有了一定的改善和提高。
本文与大家分享苏州大学附属第一医院放疗团队整理总结的局限性前列腺癌的立体定向放疗及最新研究进展,仅供各位同道交流与参考。如果您对本文内容其他补充或者建议,欢迎文末留言~~
前列腺癌体外放疗的现状
前列腺癌的放疗大体可以分为体外放疗和近距离放疗,体外放疗具有疗效好、适应证广、并发症少等优点,可以治疗各期前列腺癌,也成为了前列腺癌放疗的主流方式。
体外放疗是治疗局限性前列腺癌的主要手段之一,与手术一样,体外放疗能够达到根治效果。现代放疗技术和根治性前列腺切除术在局限性前列腺癌治疗中均可获得满意的无进展生存率。
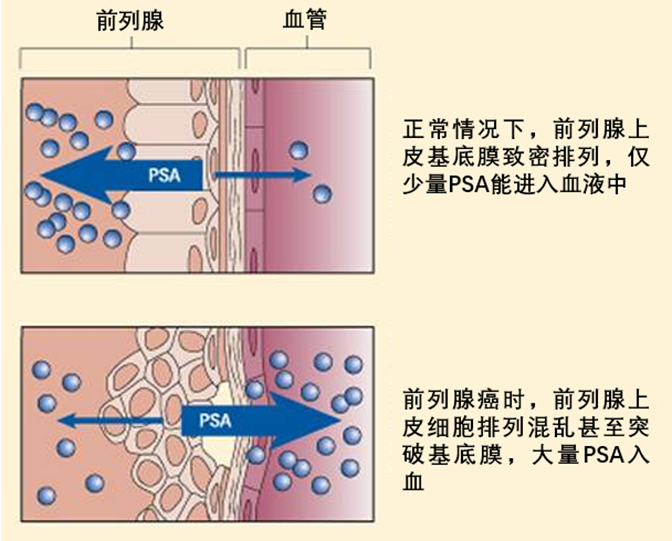
对于行前列腺癌根治术的患者,术后辅助放疗可显著降低具有复发高危因素患者的生化及临床复发风险,这些高危风险包括精囊腺受侵、前列腺包膜外侵犯、广泛切缘阳性及术后前列腺特异性抗原(prostate-specific antigen,PSA)持续升高等。
传统放疗对前列腺癌的治疗效果已经得到证实,近年来的研究表明,SBRT对局限性前列腺癌的无生化进展生存期和不良事件结局也有着较为积极的影响[12]。
这主要基于前列腺癌的一些放射生物学特性,放射生物学使用组织的α/β比值来描述放疗对组织的生物学效应,α/β比值较低的组织表现出相对较高的分割敏感性,现证实前列腺癌的α/β比值比周围器官要低。前列腺癌的这种性质使得低分割放疗在临床上可能会具有更高的治疗增益。
SBRT的有效性
与常规分割放疗相比,SBRT可以在不增加远期毒性的同时提供相似的治疗效果,并且治疗成本更低,也能够为患者提供更多的便捷,有较大的临床应用前景。
Widmark等开展的Ⅲ期临床对照研究Hypo-RT-PC是一项在斯堪的纳维亚进行的大规模试验,也是目前唯一发表的关于前列腺癌SBRT的随机对照试验。
-
在这项试验中,1200例中危和高危型局限性前列腺癌患者被随机分成两组,一组为常规分割治疗组,接受2Gy/次、共78Gy/39次、5次/周、共8周的分割治疗;另一组为SBRT治疗组,接受6.1Gy/次、共42.7Gy/7次、3次/周、共2.5周的分割治疗。
-
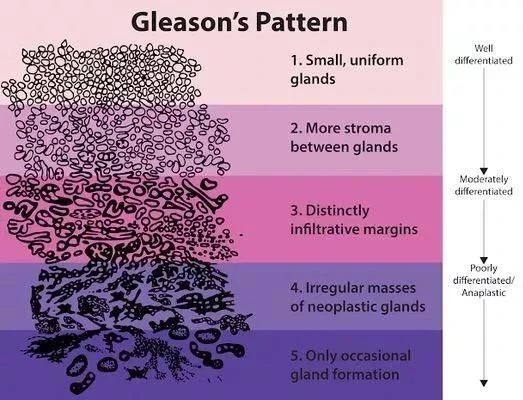
纳入患者满足以下1种或2种条件:临床分期T3a;Gleason评分≥7;10 μg/L≤PSA<20 μg/L。值得注意的是纳入患者不允许做前列腺癌的雄激素剥夺治疗(androgen deprivation therapy,ADT)。
-
试验的主要终点是患者出现生化或临床复发。
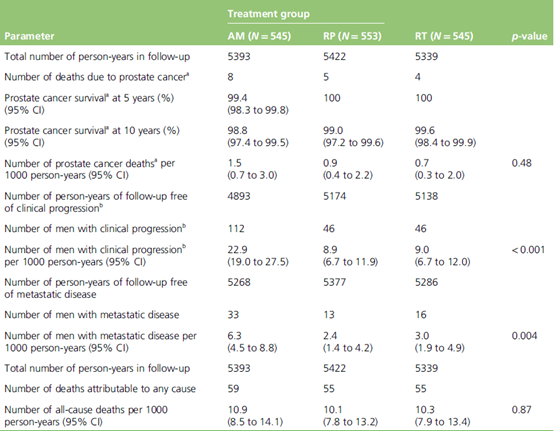
这项研究中,纳入人群中有89%是中危型前列腺癌,11%是高危型前列腺癌,研究的平均随访时间为5.0年。常规分割组和SBRT组的5年生化或临床无复发生存率均为84%(调整后HR为1.002,95%CI为0.758~1.325),由此证实SBRT方案不亚于传统分割方案。研究结果证实,SBRT的疗效与年龄、Gleason评分、临床T分期、基线PSA和风险人群在内的一些基线因素之间没有显著的相关性。
另外还发现,在以远期失败率和总存活率作为次要终点的一系列研究上,SBRT和常规分割方案具有相似的疗效。正常组织毒性反应方面,早期泌尿系反应SBRT组高于常规分割组,但晚期毒性反应两组差异无统计学意义。研究结果支持临床应用SBRT放疗技术。
Alayed等报道了一项综合分析,是关于SBRT治疗低危和中危型前列腺癌的前瞻性研究。剂量分别为35Gy/5次(计划靶区33.25Gy/5次)和40Gy/5次(计划靶区38 Gy/5次),中位随访时间分别为9.6年和6.9年,随访期间均未出现前列腺癌患者死亡。35Gy组和40Gy组5年生化复发率分别为2.5%和3.3%(P=0.78)。
Kishan等对12项Ⅱ期研究中2142例患者数据综合分析,对SBRT治疗中低危型前列腺癌患者的相关结果进行了报道。研究对象中大约55%的患者为低危型前列腺癌,32%为预后良好的中危型前列腺癌,12%为预后不良的中危型前列腺癌,大约5%的患者接受ADT,中位随访时间为6.9年。3个不同危险组患者7年内生化复发率分别为4.5%、8.6%和14.9%,总生存率分别为91.4%、93.7%和86.5%。研究结果显示放疗剂量和ADT的使用与生化复发时间的延长均无明显关系。
Jackson等对6000余例接受SBRT的患者进行了Meta分析显示,低危型和中危型患者的5年无生化进展生存率分别为96.7%和92.1%。在该研究中,生化控制和放疗处方剂量之间存在显著的相关性。这一研究中有相当比例的患者属于中等风险类别,但在中等风险人群中没有根据预后情况进行分组。
目前支持SBRT治疗高危型局限性前列腺癌的前瞻性证据很少。
Hypo-RT-PC试验中仅有11%的人群是高危人群。
Alayed等比较了两项使用SBRT治疗高危型局限性前列腺癌的前瞻性Ⅱ期试验,两个试验组选择性进行或未进行盆腔淋巴结放疗。其中一组患者接受放疗剂量为前列腺40Gy/5次,精囊30Gy/5次;另一组患者接受前列腺40Gy/5次,盆腔淋巴引流区和精囊25Gy/5次。两组的5年生化复发率分别为14.6%和0,5年总生存率分别为93.2%和96.7%(P=0.86)。提示盆腔淋巴引流区进行SBRT是可行的,盆腔淋巴引流区的照射有助于生化控制。
SBRT的毒性反应
在Widmark等开展的Ⅲ期临床对照Hypo-RT-PC中,医生采用美国放射肿瘤协作组(RTOG)发病率量表进行毒性记录,使用前列腺癌症状量表问卷进行患者生命质量评估。在治疗结束时,SBRT组与传统分割组相比,RTOG2级或更严重的急性泌尿道毒性更明显(28% vs. 23%),但这一差异在随访1年后消失。两组5年内RTOG 2级或更严重的泌尿道毒性发生率均为5%。在整个随访过程中,医生报告的RTOG 2级或更严重的胃肠道毒性的发生率在两组之间的差异没有统计学意义。在治疗结束时,患者问卷示SBRT组较传统分割组泌尿道和胃肠道症状更严重(P=0.006 6;P<0.0001),但两组间差异在随访超过2年后消失。两组患者的勃起功能没有差异。
Jackson等报告了针对SBRT的研究结果,入选的研究对象为不宜手术的低危型或预后良好的中危型前列腺癌患者(临床分期T1c-2c,Gleason评分≤3+4,PSA≤20μg/L)以及首选放疗的前列腺癌患者,入选患者不允许接受ADT治疗。
-
患者被随机分配到两组,一组是SBRT组(接受7.25Gy/次,共36.25Gy/5次,共1~2周的分割治疗),一组是常规分割(接受2Gy/次,共78Gy/39次,共7.8周的分割治疗)或中度低分割(接受3.1Gy/次,共62Gy/20次,共4周的分割治疗)方案组。
-
共有430例患者被分配到常规分割或中度低分割组(其中69%的患者接受中度低分割方案),414例患者被分配到SBRT组。
-
在两组患者中,RTOG2级或更严重的胃肠道及泌尿道毒性差异具有统计学意义。晚期毒性结果和疗效结果尚待公布。
在Kishan等进行的单臂Ⅱ期研究的综合分析中,RTOG3级或更严重的急性胃肠道和泌尿道毒性事件发生率分别为0.6%和0.09%。RTOG3级或更严重的晚期胃肠道及泌尿道毒性事件7年累计发生率分别为2.4%和0.4%。
Jackson等Meta分析结果显示,RTOG3级或更严重晚期胃肠道及泌尿道毒性发生率分别为2.0%和1.1%。
Musunuru等对两种剂量分割方案的对比评价显示,剂量从每周35 Gy/5次增加到40 Gy/5次,泌尿道毒性(5% vs. 24.2%)和胃肠道毒性(7.6% vs. 26.2%)的累积发生率升高。然而,Quon等针对相同研究的生命质量进行分析,显示在生命质量下降程度上两组间差异没有统计学意义。
Kim等观察到了类似的剂量毒性关系。在多中心进行的剂量递增Ⅱ期试验中,剂量为每周45 Gy/5次、47.5 Gy/5次和50 Gy/5次的各组,RTOG2级或更严重的晚期胃肠道毒性累积发生率分别为6.7%、33.3%和32.8%,RTOG3~4级胃肠道毒性的累积发生率分别为0、1.6%和8.2%。RTOG3级或更严重的胃肠道晚期毒性发生情况与接受至少50Gy照射的直肠体积显著相关(P<0.0001)。
Musunuru等比较了低危和中危型前列腺癌患者接受总剂量为40Gy、共行5次,频率分别为在1周内进行和隔天进行一次的两种剂量分割治疗方案的毒性和生命质量。终点是在急性期(≤12周)发生有临床意义的生命质量变化的比例。中位随访时间为4年,隔天一次剂量分割方案组急性期排尿和排便相关的生命质量较好,而2年时或最后一次随访时得到的晚期排尿和排便相关的生命质量差异无统计学意义。
总体而言,对于局限性前列腺癌来说,SBRT是一种很好的治疗方案,便捷性更高,且治疗成本更低,值得在临床进行研究和推广。
1)多中心随机试验和一些较小的单机构随机试验结果表明,从长远来看,SBRT与传统分割放疗一样有效,毒性并不会增加,且在方便患者和降低成本方面具有优势。
2)但在高危型患者中,采用放疗作为唯一的局部治疗方法可能不是最优的治疗方案。
3)放射生物学模型预测显示,与常规分割相比,SBRT应该能提高局限性前列腺癌的治愈率,但迄今为止完成的随机临床试验的结果似乎并不能证实这一点。需要开展更多关于局限性前列腺癌SBRT临床效果的研究,找寻放射生物模型和真实临床效果之间有差异的原因。